Aprendiendo sobre medicamentos genéricos (II). ¿Qué son los estudios de bioequivalencia?
La característica principal de los medicamentos genéricos es su intercambiabilidad por fármacos de marca que contienen el mismo principio activo, esto es, un medicamento genérico hará el mismo efecto en la persona que lo consume con la misma calidad, seguridad y eficacia que el de marca. Para demostrar que un medicamento genérico es perfectamente intercambiable por uno de marca, se hacen los estudios de bioequivalencia.
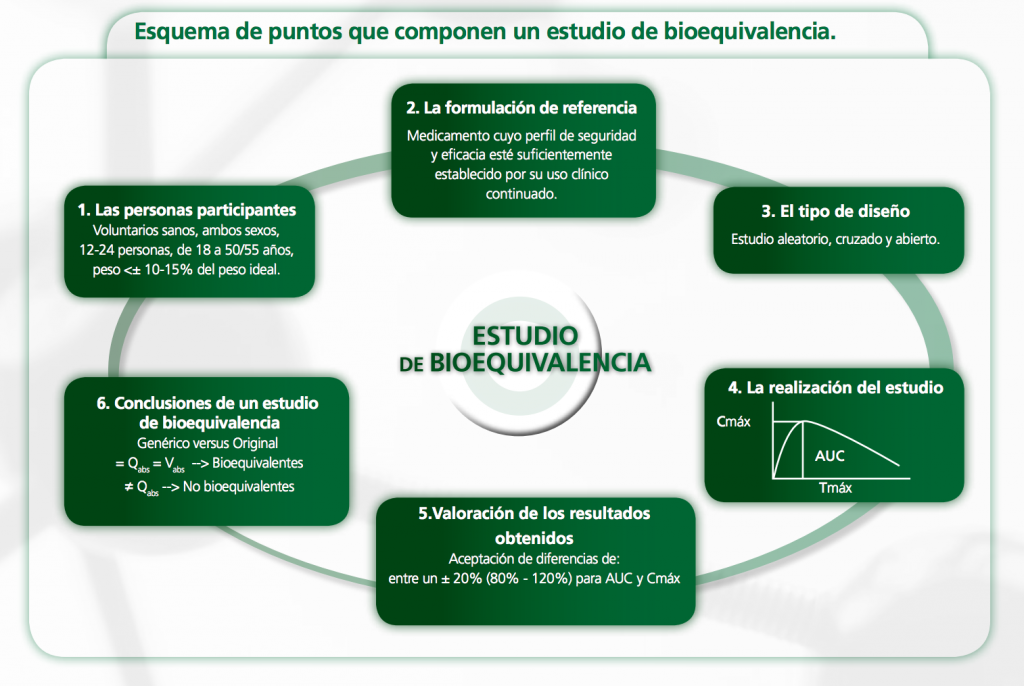
Los estudios de bioequivalencia se utilizan como herramienta para demostrar que un medicamento genérico tiene la misma eficacia terapéutica que el medicamento de referencia, existiendo entonces la posibilidad de la intercambiabilidad de uno por otro. De esta forma, se evita la realización de nuevos ensayos clínicos, que resultan muy complejos y costosos de llevar a cabo. Estos estudios se basan en el principio de que en una misma persona, si un mismo principio activo contenido en dos medicamentos similares –el equivalente genérico y el de referencia– se absorbe en la misma cantidad y velocidad en sangre, se hallará en el lugar donde ejerce la acción en una concentración similar ejerciendo entonces un efecto terapéutico también similar.
Según la Organización Mundial de la Salud (OMS) “la bioequivalencia es la relación entre dos o más productos farmacéuticos que son equivalentes farmacéuticos y muestran idéntica biodisponibilidad; por lo cual, después de administrados en la misma dosis molar son similares a tal grado, que sus efectos son esencialmente los mismos”.
Las distintas formas farmacéuticas de un mismo principio activo deben ser evaluadas de forma totalmente independiente, realizando estudios de bioequivalencia distintos para cada una de ellas. En cambio, dentro de una misma forma farmacéutica, cuando existan diferentes dosis de principio activo se puede realizar un solo estudio de bioequivalencia con una de las formulaciones, que suele ser la de la mayor cantidad en principio activo.
Se dice continuamente y erróneamente que el medicamento genérico tiene un 20% menos de principio activo, sin embargo, la realidad es muy diferente. Este 20% no significa que exista esa variabilidad en la eficacia del medicamento, ni tampoco en el contenido real de principio activo, sino que hay un 20% de variabilidad en la absorción del fármaco: de cualquier fármaco. La biodisponibilidad de cualquier principio activo varía entre los diferentes individuos e incluso a veces entre los diferentes lotes de un mismo medicamento aunque sea de marca.